
In una relazione, strategie per affrontare la nuova grande emergenza mondiale, relativa ai batteri antibiotico-resistenti
Il 19 ottobre dello scorso anno, presso l’Atahotel Expo Fiera, a Milano, si è svolta la Conferenza sul tema “Puliza e Sanificazione Sanitaria”, organizzata da PlanetHealth per conto di IIR. Tra i vari interventi, tutti di altissimo livello, Marco Ferrari, responsabile del Servizio igiene ospedaliera dell’ASST Lodi e chairman della giornata, ha svolto una relazione su come “integrare e sostenere il lavoro dell’operatore, mediante l’utilizzo di tecnologie automatizzate”, soffermando la sua attenzione su nuovi prodotti e sistemi indispensabili per affrontare la grave emergenza mondiale relativa ai Multi-drugs Resistant Organisms (MDROs), ossia i batteri antibiotico-resistenti che rischiano di costituire una piaga globale e apocalittica. Tutto il mondo scientifico è impegnato in una lotta che si rivela sempre più difficile. Anche l’Onu ha dichiarato guerra ai super batteri, impegnandosi, lo scorso ottobre, con un documento firmato dai 193 Stati membri, a definire linee guida mondiali per la lotta alla resistenza antimicrobica. Atteggiamento, questo, che affianca l’analoga attenzione al problema da parte dell’Europa.
I campanelli d’allarme
Una serie di casi “sentinella” hanno fatto scattare l’allarme. Gli scienziati del Dipartimento alla Difesa degli Stati Uniti hanno individuato, per la prima volta, un super-batterio resistente a qualsiasi tipo di antibiotici, l’Escherichia coli, nelle urine di una donna della Pennsylvania. L’agente patogeno in questione – secondo il rapporto pubblicato sulla rivista della Società americana di microbiologia «Antimicrobial Agents and Chemotherapy» – è resistente persino all’antibiotico «colistina», farmaco che spesso viene usato come ultima risorsa. Dal rapporto si evince che la donna può aver contratto il batterio anche dalla degenza ospedaliera. Questo particolare agente patogeno è stato definito dagli esperti «il batterio degli incubi», che nei casi più gravi può arrivare a una mortalità del 50% degli utenti che hanno contratto tale infezione. Alcuni ricercatori della Macquarie University di Sidney, in Australia, indagando nel campo della genomica, hanno scoperto e identificato una nuova famiglia di geni che consentirebbe ai batteri di essere immuni alla Clorexidina, il principale antisettico utilizzato negli ambienti ospedalieri. Il prototipo di gene dell’Acinetobacter baumannii, battezzato Acel, è capace di sintetizzare una proteina che riesce a rimuovere il disinfettante dalla cellula del batterio, agendo come una sorta di pompa. Geni simili ad Acel, in grado di fornire una resistenza ai disinfettanti, si trovano anche in una serie di altri batteri, compresi quelli killer. Per il 2050 si prevedono oltre 10 milioni di morti all’anno per infezione da microrganismi antibiotico resistenti, superando ampiamente i decessi per tumore (8,2 milioni), per diabete (1,5 milioni) e per incidenti stradali (1,2 milioni), con costi stimati a oltre i 100 trilioni di dollari: questo è l’allarme lanciato dal rapporto «Review on Antimicrobial Resistance» pubblicato lo scorso anno sull’Economist da Jim O’Neil, incaricato dal governo britannico di analizzare il problema e proporre soluzioni attuabili su scala globale. Nel Regno Unito, la diffusione di una nuova generazione di batteri resistenti agli antibiotici potrebbe costare la vita fino a ottantamila persone: più o meno tanti morti quanti sono stati quelli registrati a Londra durante la “grande peste” del 1665, che uccise un quinto della popolazione della città di allora. Anche l’Italia non è immune da questo rischio, anzi il nostro paese è ai primi posti in Europa per antibiotico-resistenza. Recentemente si sono evoluti ceppi capaci di resistere alla maggior parte degli antibiotici disponibili, come la Klebsiella pneumoniae, resistente ai carbapenemi. La resistenza agli antibiotici rende i batteri insensibili a questi farmaci e, nello stesso tempo, riduce le possibilità di trattamenti efficaci. Questo fenomeno tende ad essere particolarmente rilevante tra i batteri responsabili delle infezioni ospedaliere e rende molto più complicato il trattamento di queste infezioni, allungando tempi di degenza, quindi costi per il SSN, oltre ad aumentare il rischio per il paziente (affermazione del professor Gian Maria Rossolini, Direttore del Laboratorio di Microbiologia e Virologia di A.O.U. Careggi di Firenze). Secondo studi multicentrici di prevalenza, si può stimare che in Italia il 5-8% dei pazienti ricoverati contrae un’infezione ospedaliera. Ogni anno, quindi, si verificano nel nostro paese 450-700 mila infezioni in pazienti ricoverati in ospedale (soprattutto infezioni urinarie, seguite da infezioni della ferita chirurgica, polmoniti e sepsi). Di queste, si stima che circa il 30% siano potenzialmente prevenibili (135-210 mila) e che siano direttamente causa del decesso nell’1% dei casi (1350-2100 decessi prevenibili in un anno).
Gli Stati Uniti scendono in guerra
A fronte di questo quadro, gli Stati Uniti hanno messo a punto un piano strategico, per prevenire, a livello nazionale e internazionale, rilevare e controllare le malattie e le morti correlate a infezioni causate da batteri resistenti agli antibiotici, applicando misure per mitigare l’insorgenza e la diffusione di questa resistenza e assicurare la costante disponibilità di terapie per il trattamento delle infezioni batteriche. Secondo questo piano, gli sforzi dovranno concentrarsi per conseguire, entro il 2020 ambiziosi obiettivi:
• ridurre del 50% l’incidenza di infezioni da Clostridium difficile rispetto al 2011;
• ridurre del 60% le infezioni da Enterobatteri resistenti ai carbapenemi acquisite durante il ricovero ospedaliero, rispetto al 2011;
• ridurre del 35% le infezioni da Pseudomonas spp multiresistenti acquisite durante il ricovero rispetto al 2011;
• ridurre di almeno il 50% le infezioni del sangue da Staphylococcus aureus methilicin-resistenti (MRSA) rispetto al 2011;
• ridurre del 25% le infezioni da Salmonella non tifoidea multi-resistenti rispetto al 2010-2012; • ridurre del 15% il numero di infezioni I multiresistenti;
• ridurre di almeno il 25% il tasso di malattia pneumococcica invasiva resistente agli antibiotici tra i pazienti inferiori ai 5 anni di età rispetto al 2008;
• ridurre di almeno il 25% il tasso di malattia pneumococcica invasiva resistente agli antibiotici tra i pazienti superiori ai 65 anni di età rispetto al 2008.
Uno studio pubblicato il 19 ottobre scorso da Plos Medicine stima che l’impatto di sei infezioni correlate all’assistenza (polmonite, infezioni del tratto urinario, infezioni del sito chirurgico, infezioni da Clostridium difficile, sepsi neonatale e infezioni del sangue) sia superiore a quello di malattie come l’influenza, le infezioni da Hiv/Aids e la tubercolosi insieme. Nell’Unione europea, infatti, ogni anno si verificano più di 2,5 milioni di casi di infezioni nosocomiali, che si traducono in circa 2,5 milioni di anni di vita persi a causa della disabilità (Daly, Disability Adjusted Life Year).
In attesa che la scienza e la ricerca trovino una soluzione radicale sul piano clinico, occorre cercare di limitare i danni, mettendo in atto tutte le metodiche possibili per contenere al massimo la diffusione dei microrganismi e, di conseguenza, limitare la propagazione delle infezioni. Qui entrano in gioco l’igiene, la pulizia e la sanificazione ambientali, veri e propri ausili strettamente connessi all’azione più propriamente terapeutica. Questa è la sfida che quotidianamente devono affrontare, nelle strutture sanitarie, i responsabili infettivologi, gli economi, gli operatori che devono tenersi aggiornati sulle più avanzate tecnologie, cercando di coniugare, data l’attuale negativa congiuntura economica, il contenimento della spesa e il conseguimento della massima qualità per garantire la tutela della salute dei pazienti. I più esposti al rischio di contrarre infezioni ospedaliere sono essenzialmente pazienti immunocompromessi, nei quali le ICA insorgono durante il ricovero e la degenza o, in qualche caso, anche dopo la dimissione e possono avere diverso grado di gravità, fino ad essere letali. Le ICA possono interessare anche gli operatori sanitari che lavorano a contatto con i pazienti, e quindi devono essere adottate misure adeguate non solo per trattare le persone ricoverate ma anche per prevenire la diffusione delle infezioni tra il personale che fornisce assistenza e cura.
Lavare le mani
In primo luogo deve essere prestata particolare attenzione all’igiene delle mani, perché la trasmissione crociata di microrganismi si verifica soprattutto attraverso le mani degli operatori. I fattori che influenzano il trasferimento da superficie a superficie e quindi il tasso di contaminazione crociata sono: il tipo di il tipo di microrganismo, le caratteristiche delle superfici contaminate, il livello di umidità e la quantità di contaminanti. La flora transitoria si rimuove più facilmente con il lavaggio corretto delle mani. I batteri patogeni più spesso ritrovati sulle mani degli operatori sono: Staphylococcus aureus, Enterococcus faecium e, in corso di epidemie, anche Acinetobacter, Staphylococcus aureus resistente alla meticillina (MRSA) ed Enterococcus resistente alla vancomicina (VRE). Pertanto, l’igiene delle mani è senza dubbio la pratica più importante quanto a combinazione di efficacia, semplicità e costi di applicazione. Infatti il solo lavaggio delle mani può ridurre significativamente i decessi conseguenti alle infezioni, le giornate di ricovero e le spese sanitarie. (fonte IPASVI). Il passo successivo è l’accurata detergenza di superfici e attrezzature, effettuata secondo protocolli definiti in sede di assegnazione delle attività di pulizia.
Tecniche di disinfezione
Il passo successivo è l’operazione delicatissima della disinfezione. A disposizione degli operatori oggi ci sono diverse possibilità.
Panni impregnati
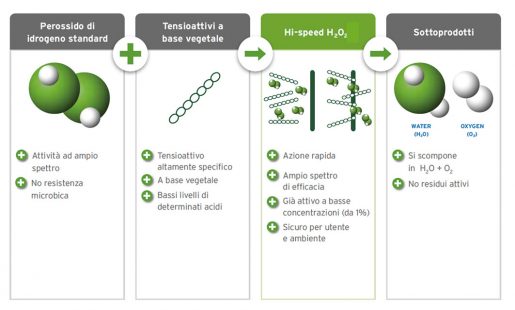
Per esempio, le procedure “touch”, ossia panni monouso impregnati con perossido di idrogeno, che garantiscono il rilascio ottimale del disinfettante, non consentono alcun errore legato a insufficiente quantità o errata preparazione del disinfettante (ad esempio diluizione/durezza e contaminazione microbica dell’acqua), non creano problemi legati alla contaminazione da refilling, causano minore inalazione ed esposizione dermica ai componenti. O le procedure “touch” riprocessabili abbinate a tecnologie che utilizzano il perossido di idrogeno “Hi-speed”. La combinazione con tensioattivi altamente specifici dei prodotti permette al perossido d’idrogeno di entrare più velocemente nei microorganismi, sinergizzando le sue caratteristiche di forte antiossidante microbico, riducendo di conseguenza i tempi di contatto, a concentrazioni d’uso nettamente inferiori (1-1,5%) rispetto al perossido standard (≈8%). Non agiscono, però, sulle spore.
Il perossido d’idrogeno
Ci sono poi tecnologie automatizzate di disinfezione a base di perossido d’idrogeno “no touch”. Si tratta di interventi complementari alla detersione e all’eventuale disinfezione “touch”. La procedura consiste nella micro nebulizzazione di perossido di idrogeno in ambienti confinati, in assenza di pazienti e operatori, mantenendo nella stanza le attrezzature e i presidi pluriuso. Il perossido di idrogeno innesca un meccanismo ossidante, che inattiva i microrganismi patogeni attraverso un radicale libero idrossile, che intacca la componente lipidica delle membrane oltre al Dna delle cellule dei batteri. I cationi dell’argento potenziano l’azione battericida nei confronti di batteri, virus, miceti e spore. Al termine dell’erogazione i radicali liberi del perossido di idrogeno si trasformano in ossigeno, per cui non rimane alcun residuo nell’aria dell’ambiente trattato. L’intervento è ripetibile, indifferentemente dall’affidabilità degli operatori, e viene effettuato con l’utilizzo di apparecchi tecnologicamente evoluti. L’efficacia della procedura è supportata da ampia letteratura che dimostra l’eradicazione dei MDROs, spore comprese. Il “Cavallo di Troia” Esistono anche disinfettanti a largo spettro battericida, substrati metabolici antimicrobici, che legano debolmente ioni d’argento a ioni di acido citrico. I microbi riconoscono gli ioni di argento in acido citrico come una sorgente di cibo. Le proteine di trasporto attraversano la membrana cellulare e trasportano differenti molecole, appartenenti in genere a due categorie: nutrienti e sostanze endogene necessarie al funzionamento cellulare. Nel caso dei batteri, le proteine di trasporto riconoscono l’acido citrico come un alimento e lo trasferiscono quindi nel microrganismo. Una volta penetrato al suo interno i cationi di argento si comportano come veri e propri “cavalli di Troia”, ossia reagiscono rapidamente con i gruppi di carica negativa, causando danni irreversibili sia alle proteine che al DNA e al RNA dei batteri bloccandone le funzioni metaboliche e riproduttive sino alla loro inattivazione.
La luce
Anche i Raggi UV-C rigenerati, emessi da lampade a vapori di mercurio o da lampade a vapori di gas xenon possono essere utilizzati in funzione sterilizzante. Si tratta di raggi ultravioletti con lunghezza d’onda compresa tra 100 e 280 nanometri, che possiedono proprietà germicide, parziale nei confronti delle spore. Il trattamento con i Raggi UV-C deve essere effettuato in assenza di persone, in quanto non è ancora chiaro quali possano essere le conseguenze in caso di esposizione accidentale. I cicli di erogazione devono essere ripetuti più volte nei locali da trattare, con tempi diversi a seconda del MDROs su cui si vuole agire, variando la posizione della fonte di emissione. I raggi non agiscono attraverso plastica, vetro e tessuti. Inoltre, non è ancora chiaro l’impatto che possono avere sui materiali ospedalieri.
Foto ossidazione
È un sistema di purificazione dell’aria, non solo di quella che attraversa il catalizzatore, ma anche di quella presente nell’ambiente, in quanto vi immettono una fitta coltre di molecole Ros (Reactive Oxygen Species – Specie reattive dell’ossigeno), che producono una nebbia di ioni di idrossido, radicali, radicali perossidi, idroperossidi che, attraverso l’azione della luce e dell’umidità dell’aria, attivano una reazione di decomposizione delle sostanze organiche e inorganiche nocive, lasciando solo ossigeno e molecole di idrogeno. I depuratori riducono rapidamente i contaminanti a base di carbonio.






